禮來啟動(dòng)全球首項(xiàng)抗體療法臨床試驗(yàn)
禮來公司(Lilly)今日宣布����,該公司與AbCellera聯(lián)合開發(fā)的新冠病毒中和抗體LY-CoV555���,已經(jīng)在1期臨床試驗(yàn)中完成首例患者給藥����。新聞稿指出����,這是全球首項(xiàng)針對(duì)COVID-19的潛在抗體療法的人體臨床試驗(yàn)。
LY-CoV555是一款靶向新冠病毒的刺突蛋白(S protein)的強(qiáng)效中和抗體�����,它旨在阻斷新冠病毒進(jìn)入細(xì)胞的過程����。這款在研抗體是從第一批美國(guó)COVID-19康復(fù)患者的血樣中分離開發(fā)而成。在抗體最初發(fā)現(xiàn)之后�����,禮來公司的科學(xué)家在短短三個(gè)月內(nèi)就迅速研制出了這一抗體療法。名為J2W-MC-PYAA的臨床試驗(yàn)是一項(xiàng)隨機(jī)雙盲����、含安慰劑對(duì)照的1期臨床試驗(yàn),旨在研究LY-CoV555在因COVID-19住院的患者中單次給藥后的安全性�����、耐受性�����、藥代動(dòng)力學(xué)(PK)和藥效學(xué)(PD)����。預(yù)計(jì)這項(xiàng)試驗(yàn)的結(jié)果將在6月底獲得。如果1期研究結(jié)果顯示可以安全使用抗體����,禮來公司預(yù)計(jì)將進(jìn)入下一階段的測(cè)試,在非住院的COVID-19患者中檢測(cè)LY-CoV555的效果�����。該公司還計(jì)劃在預(yù)防性環(huán)境下研究該藥物,重點(diǎn)關(guān)注那些歷史上不是疫苗最佳候選者的脆弱患者人群����。

藥明康德內(nèi)容團(tuán)隊(duì)制圖
“諸如LY-CoV555之類的抗體療法可能對(duì)預(yù)防和治療COVID-19具有雙重潛力�����,并且對(duì)于遭受疾病打擊最嚴(yán)重的人群���,例如老年人和免疫系統(tǒng)受損的人群可能特別重要����?��!盠illy首席科學(xué)官�����、禮來研究實(shí)驗(yàn)室總裁Daniel Skovronsky博士說����,“在研究安全性和有效性的同時(shí)����,我們也開始大規(guī)模生產(chǎn)這種潛在的療法����。如果LY-CoV555成為COVID-19近期解決方案的一部分�����,我們希望盡快將其提供給患者����,目標(biāo)是在年底前獲得數(shù)十萬劑藥物?��!?/span>禮來公司同時(shí)還與君實(shí)生物達(dá)成合作�����,聯(lián)合開發(fā)靶向新冠病毒的中和抗體�����。日前�����,雙方聯(lián)合開發(fā)的候選抗體在恒河猴動(dòng)物實(shí)驗(yàn)中證實(shí)其預(yù)防和治療潛力���。雙方計(jì)劃在第二季度推進(jìn)抗體的臨床申請(qǐng)工作�����。禮來計(jì)劃在接下來的幾個(gè)月里測(cè)試多種新冠病毒中和抗體作為單藥,或作為抗體雞尾酒療法���,治療COVID-19患者的作用���。吉利德科學(xué)公布瑞德西韋治療中度新冠肺炎患者結(jié)果
今天,吉利德科學(xué)(Gilead Sciences)宣布了其抗病毒藥物瑞德西韋(remdesivir)���,在治療中度新冠肺炎住院患者時(shí)的臨床試驗(yàn)結(jié)果�����。在這一開放標(biāo)簽3期臨床試驗(yàn)中�����,5天療程的瑞德西韋聯(lián)合標(biāo)準(zhǔn)護(hù)理���,在接受治療后第11天�����,將患者臨床改善的可能性提高65%(OR=1.65���,95% CI,1.09-2.48���,p=0.017)���。瑞德西韋10天療程與標(biāo)準(zhǔn)治療相比,對(duì)臨床改善的幾率也提供益處�����,但未達(dá)到統(tǒng)計(jì)學(xué)顯著性����。該公司計(jì)劃在未來幾周內(nèi)將全部數(shù)據(jù)提交到同行評(píng)議的期刊上發(fā)表。
此前����,瑞德西韋治療嚴(yán)重新冠肺炎的多項(xiàng)3期臨床試驗(yàn)數(shù)據(jù)已經(jīng)獲得發(fā)表���。這一試驗(yàn)的不同之處是治療中度新冠肺炎患者,定義為雖然確診患有新冠肺炎并且住院接受治療�����,但是不需要接受機(jī)械通氣�����,而且呼吸空氣時(shí)血氧飽和度大于94%�����。它們以1:1:1的比例隨機(jī)接受瑞德西韋5天或10天療程的治療���,或標(biāo)準(zhǔn)護(hù)理。主要終點(diǎn)為在接受治療后第11天�����,使用7級(jí)評(píng)分評(píng)估的臨床狀態(tài)����。7級(jí)評(píng)分的范圍從出院到增加氧氣和通氣支持水平���,直至死亡。試驗(yàn)結(jié)果表明����,在接受治療后第11天,與標(biāo)準(zhǔn)護(hù)理組相比����,5天療程治療組中達(dá)到臨床狀態(tài)改善的患者比例顯著提高。此外����,接受瑞德西韋治療的患者臨床狀態(tài)惡化或死亡的數(shù)目比標(biāo)準(zhǔn)護(hù)理組有所減少,但是未達(dá)到統(tǒng)計(jì)學(xué)顯著性���。
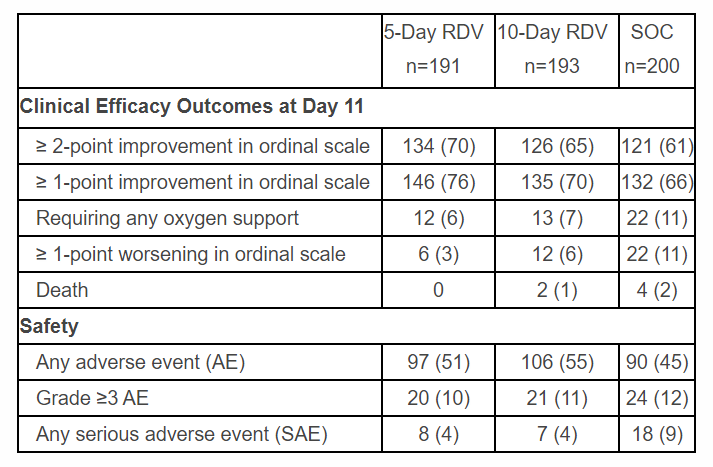
▲這一研究的關(guān)鍵療效和安全性結(jié)果(圖片來源:參考資料[2])
“我們現(xiàn)在有多個(gè)隨機(jī)����,對(duì)照的臨床試驗(yàn)證明瑞德西韋在治療不同患者類型時(shí)改善了臨床結(jié)果����。今天的結(jié)果顯示,當(dāng)治療中度疾病時(shí)�����,5天療程的remdesivir比標(biāo)準(zhǔn)治療帶來了更大的臨床改善?���!奔驴茖W(xué)首席醫(yī)學(xué)官M(fèi)erdad Parsey博士說:“我們今天掌握的額外數(shù)據(jù)將進(jìn)一步指導(dǎo)我們的研究工作,包括在疾病更早階段評(píng)估療法的效果����,與其他療法聯(lián)用治療最危重患者,兒科研究和開發(fā)替代劑型���?��!?/span>
參考資料:
[1] Gilead Announces Results From Phase 3 Trial of Remdesivir in Patients With Moderate COVID-19. Retrieved June 1, 2020, from https://www.gilead.com/news-and-press/press-room/press-releases/2020/6/gilead-announces-results-from-phase-3-trial-of-remdesivir-in-patients-with-moderate-covid-19
[2] Lilly Begins World's First Study of a Potential COVID-19 Antibody Treatment in Humans. Retrieved June 1, 2020, from https://investor.lilly.com/news-releases/news-release-details/lilly-begins-worlds-first-study-potential-covid-19-antibody



