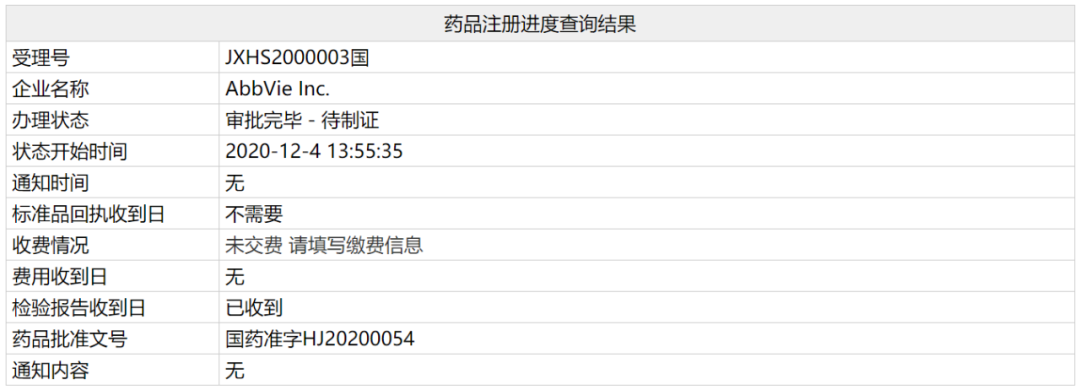
12月4日晚間�,中國國家藥監(jiān)局官網(wǎng)信息顯示���,艾伯維(AbbVie)與羅氏(Roche)共同開發(fā)的BCL-2抑制劑維奈克拉片(venetoclax��,ABT-199)的上市申請受理號已更新為“審批完畢-待制證”��,并發(fā)布了批準文號��。這意味著這款藥物已經(jīng)在中國獲批�。根據(jù)早前信息�,此次獲批適應(yīng)癥為,聯(lián)合其它藥物用于治療年齡75歲及以上���,或因合并癥不適于接受強誘導(dǎo)化療的新診斷的成人急性髓性白血?����。ˋML)患者�。公開資料顯示���,維奈克拉是全球首個獲得批準上市的BCL-2抑制劑����,自問世以來曾5次被美國FDA授予突破性療法認定���。本次獲批意味著這款突破性療法終于惠及到中國患者��,同時也標志著維奈克拉成為了首個在中國獲批上市的BCL-2抑制劑��。
BCL-2(B細胞淋巴瘤因子)是一種癌基因����,具有抑制細胞凋亡的作用�����。BCL-2家族蛋白于上世紀80年代被發(fā)現(xiàn)����,它通過與促凋亡蛋白BIM、BAD等形成二聚體以及自身二聚��,在細胞凋亡的調(diào)控中發(fā)揮重要作用���。但是研究發(fā)現(xiàn)�,在有些血癌中��,BCL-2蛋白的積累會導(dǎo)致腫瘤細胞無法進入細胞凋亡過程�����。此外,BCL-2蛋白的過度表達也與耐藥性的形成有關(guān)���。因此���,BCL-2蛋白成為了血液癌癥治療的一個新靶標。然而���,以BCL-2為靶點的創(chuàng)新藥物研發(fā)并不順利�����。直到BCL-2蛋白被發(fā)現(xiàn)的三十年后�,人類才迎來了首款獲批的BCL-2抑制劑�����,它就是本次在中國獲批的維奈克拉片�。維奈克拉是艾伯維與羅氏共同開發(fā)的一款“first-in-class”口服、選擇性BCL-2抑制劑�����,它可通過選擇性抑制BCL-2功能,重塑細胞的關(guān)鍵信號通路�,讓癌細胞自我毀滅���,達到治療腫瘤的目的�����。2016年4月�����,維奈克拉在美國獲批����,成為了全球首個獲批準上市的BCL-2抑制劑�。目前,維奈克拉已在美國獲批治療慢性淋巴細胞白血?���。–LL)、小淋巴細胞性淋巴瘤(SLL)���、急性骨髓性白血病等多種適應(yīng)癥��。由于維奈克拉治療效果突出�����,FDA曾先后多次授予其突破性療法認定����。在中國,維奈克拉的上市申請在2020年1月獲得CDE受理����,并在今年2月因“具有明顯治療優(yōu)勢創(chuàng)新藥”被納入優(yōu)先審評。該藥本次獲批的適應(yīng)癥為:與阿扎胞苷�,或地西他濱,或低劑量阿糖胞苷聯(lián)用適于治療年齡75歲及以上�,或因合并癥不適于接受強誘導(dǎo)化療的新診斷的成人AML患者。根據(jù)在維奈克拉在美國獲批時的臨床試驗數(shù)據(jù)��,維奈克拉聯(lián)合療法在治療這類AML患者中具有良好的療效和安全性�����。在M14-358試驗中�����,接受維奈克拉和阿扎胞苷組合療法治療的AML患者的完全緩解率(CR)為37%,完全緩解兼部分血細胞計數(shù)緩解率(CRh)為24%�。接受維奈克拉和地西他濱組合療法治療的患者的CR為54%,CRh為8%��。M14-387試驗結(jié)果表明�,維奈克拉與低劑量阿糖胞苷聯(lián)用��,患者CR為21%��,CRh為21%�����。今年8月發(fā)表在《新英格蘭醫(yī)學(xué)雜志》上的一篇研究顯示��,維奈克拉與阿扎胞苷聯(lián)用在一線治療無法接受高強度化療的AML患者的3期臨床試驗中達到了主要臨床終點:與阿扎胞苷單藥治療相比�,聯(lián)合療法將患者死亡風(fēng)險降低34%,顯著延長了患者的總生存期(OS)�����。AML是最常見的急性白血病���,發(fā)病者多為老年人�����。目前�,對AML的標準治療是強力誘導(dǎo)化療,然后進行鞏固化療或者同種異體干細胞移植���。然而��,由于年齡��、合并癥��、以及攜帶不良基因突變等原因�����,很多老年患者無法接受標準化療或者對它們產(chǎn)生耐藥性���。維奈克拉的到來,為這些患者提供了新的選擇���。本次在中國獲批意味著�����,這款突破性療法終于可以惠及到中國AML患者��,幫助他們改善生活質(zhì)量�。值得一提的是,除了本次獲批的適應(yīng)癥�,目前維奈克拉已在中國獲批多項臨床研究,涉及的適應(yīng)癥包括慢性淋巴細胞性白血病成人患者��、常規(guī)化療后首次緩解的急性髓性白血病患者���、異基因干細胞移植后的急性髓性白血病患者等等。期待這些臨床研究也順利進行�����,讓維奈克拉惠及到更多的白血病患者��。





