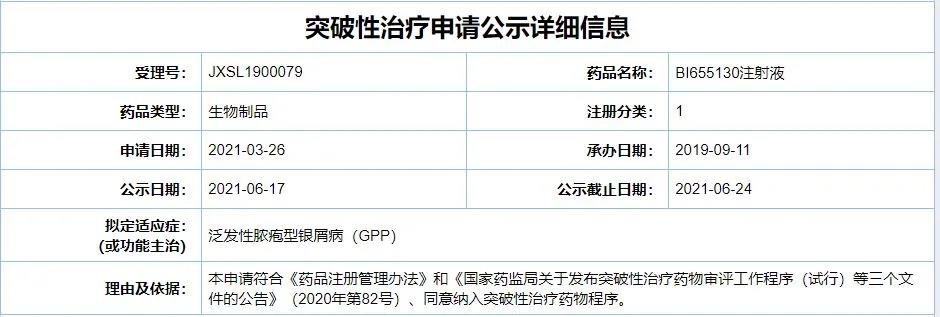
根據(jù)中國國家藥品監(jiān)督管理局藥品審評中心(CDE)公示,勃林格殷格翰(Boehringer Ingelheim)的IL-36R單抗BI 655130(spesolimab)注射液已于6月17日被納入擬突破性治療品種,擬定適應(yīng)癥為泛發(fā)性膿皰型銀屑?�。℅PP)��。公開資料顯示��,BI655130是一款“first-in-class”在研新藥��,全球范圍內(nèi)已進入3期臨床試驗階段��。
IL-36成員是樹突細胞和T細胞的強效調(diào)節(jié)劑���,在免疫調(diào)理及免疫激活作用中參與樹突細胞與Th細胞的激活��、抗原提呈和刺激促炎因子產(chǎn)生��。研究表明��,IL-36在皮膚中大量表達���,并在銀屑病等皮膚病發(fā)病機制中扮演重要角色。BI 655130是勃林格殷格翰開發(fā)的一款靶向IL-36受體的單克隆抗體��,可阻斷白細胞介素-36受體(IL-36R)的作用���,具有治療皮膚病���、掌跖膿皰病、潰瘍性結(jié)腸炎等多種炎癥性疾病的潛力���。在中國���,BI 655130已獲批多項臨床試驗,涉及的適應(yīng)癥包括急性或慢性泛發(fā)性膿皰性銀屑病���、泛發(fā)性膿皰性銀屑病等���。本次,BI 655130被納入擬突破性治療品種的適應(yīng)癥為泛發(fā)性膿皰型銀屑病���。中國藥物臨床試驗登記與信息公示平臺顯示��,BI 655130正在開展多項針對泛發(fā)性膿皰型銀屑病的臨床試驗���,其中包括一項開放、非隨機化���、單臂國際多中心3期臨床試驗��,以及一項隨機��、雙盲的國際多中心2期臨床���。BI 655130治療泛發(fā)性膿皰型銀屑病的療效已在臨床試驗中得到初步驗證��。根據(jù)2019年3月發(fā)表在《新英格蘭醫(yī)學(xué)雜志》(NEJM)上的1期臨床研究數(shù)據(jù)���,BI 655130可顯著改善泛發(fā)性膿皰性銀屑病的癥狀。數(shù)據(jù)顯示:7名經(jīng)歷急性中重度疾病發(fā)作的泛發(fā)性膿皰性銀屑病患者在使用BI 655130后��,癥狀得到了快速改善��;在為期20周的這項1期臨床試驗中��,7名患者中的5人在單劑量治療后的第一周內(nèi)便達到皮膚清除或接近清除���,其他患者在4周后也都達到了同樣效果���;在第4周,患者皮膚癥狀的平均改善程度接近80%��,且一直維持到研究結(jié)束(第20周)。泛發(fā)性膿皰性銀屑病是一種罕見的慢性皮膚病��,可對患者的生活質(zhì)量產(chǎn)生巨大的影響���?��;颊咴诨疾『笃つw會變紅���,并在身體各區(qū)域爆發(fā)出許多無菌性的膿皰��。泛發(fā)性膿皰性銀屑病患者可能會出現(xiàn)突然發(fā)熱���、寒戰(zhàn)和皮膚疼痛性病變的癥狀。該疾病可能伴有危及生命的器官衰竭和感染性并發(fā)癥��。目前��,泛發(fā)性膿皰性銀屑病的治療方案極為有限���,且缺乏深入��、持久療效���。因此泛發(fā)性膿皰性銀屑病患者對快速���、強效且持久的新治療選擇有著迫切的需求。期待BI 655130的后續(xù)研究順利進行���,早日為患者帶來新的治療選擇���。





