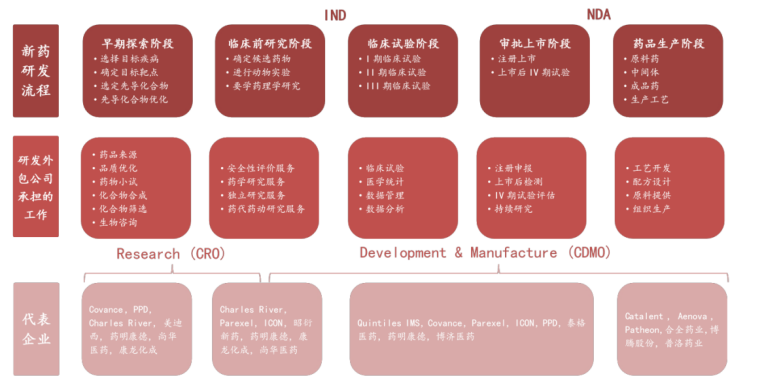
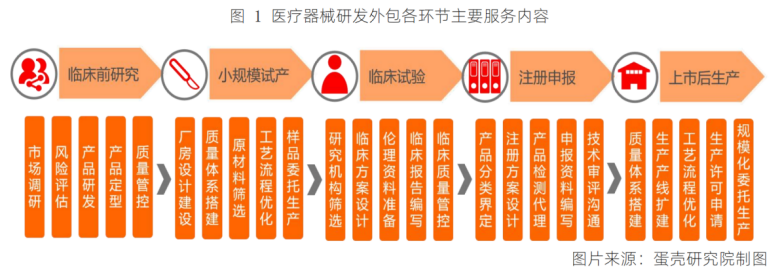
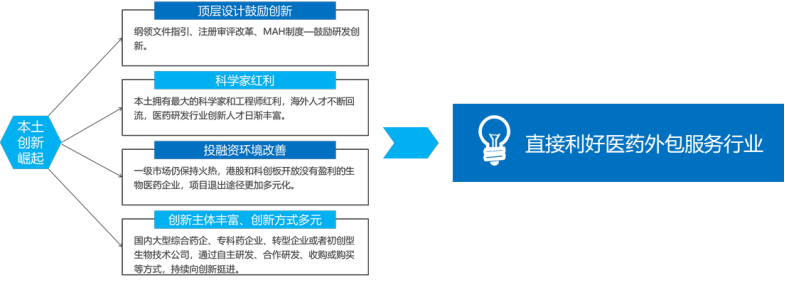
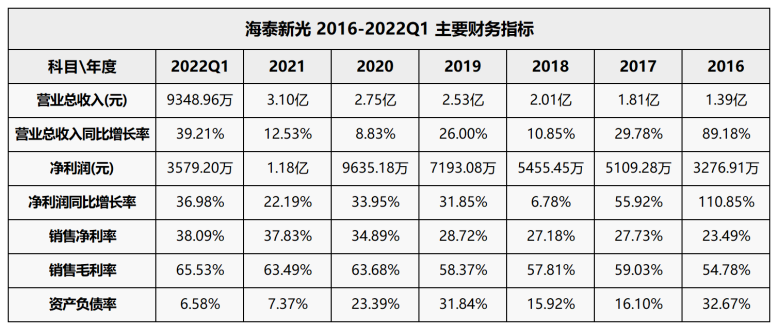
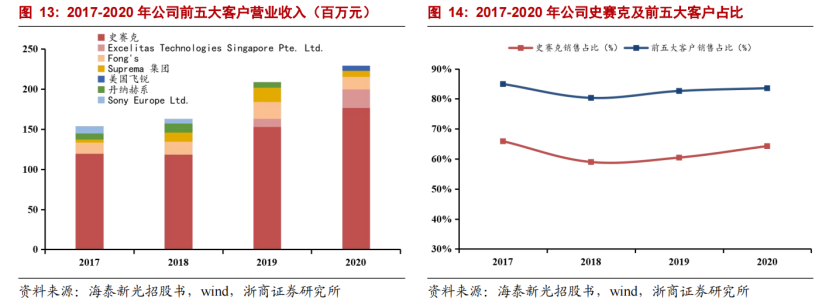
隨著醫(yī)藥CXO行業(yè)誕生了許多市值過百億甚至超千億的公司,這兩年醫(yī)療器械外包行業(yè)一級市場融資也變得十分火熱���,但上市公司卻寥寥無幾。究竟醫(yī)療器械外包市場前景如何����,存在哪些行業(yè)痛點和發(fā)展契機?又有哪些企業(yè)能夠從中突圍呢�����?近年來����,隨著國內創(chuàng)新藥行業(yè)迎來“黃金時代”,在研新藥數(shù)量和醫(yī)藥投入不斷增多���,不僅帶動了醫(yī)藥外包(CXO)行業(yè)加速發(fā)展�����,還誕生了許多市值過百億甚至超千億的公司����,例如泰格醫(yī)藥�����、藥明康德、康龍化成���、藥明生物等。CXO為醫(yī)藥外包的統(tǒng)稱���,主要分為CRO(研發(fā)外包)�����、CMO/CDMO(生產(chǎn)外包)�����、CSO(銷售外包)三個環(huán)節(jié)�����,為醫(yī)藥企業(yè)提供三種不同的服務�����。(醫(yī)藥研發(fā)外包服務的環(huán)節(jié) 數(shù)據(jù)來源:西南證券)實際上���,不只醫(yī)藥環(huán)節(jié)可以外包���,醫(yī)療器械行業(yè)同樣有外包服務,包括醫(yī)療器械CRO(合同研究組織)�����、醫(yī)療器械CDMO(合同研發(fā)生產(chǎn)組織)等���。近年來醫(yī)藥CXO賽道成為牛股集中營���、在資本市場備受熱捧。受此影響���,這兩年醫(yī)療器械外包公司在一級市場的融資也呈現(xiàn)出火熱態(tài)勢����。例如����,2021年7月,巨翊科技完成逾億元B輪融資����,將用于加速醫(yī)療器械CDMO能力建設與醫(yī)工轉化布局�����,并推進相關業(yè)務的進一步發(fā)展���;醫(yī)療器械技術轉化服務提供商致眾科技也完成了數(shù)千萬元A+輪融資,將重點布局醫(yī)療器械CRO+CDMO�����。2022年5月���,領伯醫(yī)匯完成數(shù)千萬元PreA輪融資,加快醫(yī)療器械版塊CDMO和CMO平臺建設�����,整體服務能力將滿足80%以上走注冊人制度上市的器械產(chǎn)品的受托生產(chǎn)需求���;介入醫(yī)療器械CDMO昊豐醫(yī)療也完成了數(shù)千萬元Pre-A輪融資����,將用于CDMO平臺中高分子材料平臺的搭建、產(chǎn)能擴充和人才招募���。不過����,相比于在二級市場受資本熱捧的醫(yī)藥CXO賽道����,醫(yī)療器械外包市場的火熱程度顯得十分遜色。百億賽道����,醫(yī)療器械外包市場前景如何?為何醫(yī)療器械外包上市公司寥寥無幾�����,究竟行業(yè)前景如何���?實際上����,醫(yī)療器械外包與醫(yī)藥外包存在一定的異同點���。兩者類似的地方在于:其一�����,都是為各自的服務對象提供研發(fā)外包服務�����,幫助客戶降低研發(fā)風險�����、提高研發(fā)效率���、減少成本投入、加快審批流程�����、優(yōu)化生產(chǎn)工藝���;其二���,在外包服務環(huán)節(jié)上也有類似之處����,醫(yī)療器械研發(fā)外包服務主要覆蓋臨床前研究���、小規(guī)模試產(chǎn)���、臨床試驗、注冊申報和上市后生產(chǎn)5個環(huán)節(jié)����;其三,兩者的經(jīng)營模式都可以根據(jù)服務環(huán)節(jié)的不同�����,劃分為CRO����、CMO/CDMO或者包含多種業(yè)務的一體化服務(CXO)企業(yè)。對于醫(yī)療器械外包公司而言���,醫(yī)療器械CRO主要向醫(yī)療器械研發(fā)主體提供產(chǎn)品臨床研究服務�����,以臨床試驗為核心服務���,與臨床CRO龍頭泰格醫(yī)藥類似�����,都能幫助客戶加快臨床試驗進程����,更快地進入注冊申報環(huán)節(jié)�����。例如����,國內有從事產(chǎn)品臨床研究服務的醫(yī)療器械CRO公司���,包括泰格醫(yī)藥全資子公司泰格捷通����、奧咨達���、致眾科技�����、永銘誠道����、盛恩醫(yī)藥、邁迪思創(chuàng)����、銳意科盛、匯通醫(yī)療等�����。醫(yī)療器械CDMO主要向醫(yī)療器械研發(fā)主體提供工藝研發(fā)設計���、生產(chǎn)服務�����,主要集中在小規(guī)模試產(chǎn)和上市后生產(chǎn)環(huán)節(jié)�����,與國內CDMO龍頭藥明生物���、凱萊英類似�����,都能幫助客戶提高質量管控�����、縮短試產(chǎn)周期���、降低生產(chǎn)成本和提高生產(chǎn)效率。例如�����,海泰新光�����、巨翊科技���、領伯醫(yī)匯����、昊豐醫(yī)療等���,都有從事醫(yī)療器械CDMO業(yè)務���。但是,醫(yī)療器械外包與醫(yī)藥外包又有著本質的區(qū)別���,這也決定了兩者在市場空間�����、行業(yè)驅動因素�����、成長前景等方面根本性的不同����。首先�����,服務對象不同。醫(yī)藥外包企業(yè)面向的是國內外知名醫(yī)藥研發(fā)企業(yè)����,而醫(yī)療器械外包企業(yè)面向的是醫(yī)療器械研發(fā)主體(醫(yī)療器械研發(fā)企業(yè)、醫(yī)療器械科研院所�����、醫(yī)院科技成果轉化中心����、科研人員等)。其次�����,訂單規(guī)模相差極大���。由于新藥研發(fā)投入大(超過10億美元)�����、周期長(大約12年)�����、風險高(失敗概率大)���,藥企對外包的需求極大,更舍得花錢���,因此CRO或CDMO訂單金額一般能達到億元甚至十幾億元級別����。反過來����,由于醫(yī)療器械生產(chǎn)上的產(chǎn)業(yè)鏈相比醫(yī)藥行業(yè)成熟,定制化的需求比較低����,而且外包訂單規(guī)模小(一般在百萬或者千萬級別)���。最后����,從市場空間看,醫(yī)藥行業(yè)的市場空間遠遠高于醫(yī)療器械行業(yè)����。2019年,我國醫(yī)藥行業(yè)市場規(guī)模達1.6萬億元���,而同期我國醫(yī)療器械行業(yè)市場規(guī)模僅有6200多億元����。同時�����,2019年�����,我國CRO和CMO/CDMO市場規(guī)模分別達到814億元���、441億元����,而根據(jù)蛋殼研究院數(shù)據(jù)顯示���,2019年全國醫(yī)療器械研發(fā)外包服務行業(yè)市場規(guī)模僅為100億元���,而且市場高度分散�����,企業(yè)規(guī)模也較小。實際上����,無論訂單規(guī)模,還是市場空間之間的差異�����,都與醫(yī)療器械外包行業(yè)存在的痛點密切相關����。MAH制度落地,能否解決醫(yī)療器械外包行業(yè)痛點�����?回顧過去我國醫(yī)藥行業(yè)的歷史進程�����,之所以近年來醫(yī)藥外包行業(yè)得以快速發(fā)展,主要原因在于政策推動(MAH制度����、審評審批制度的改革等)、創(chuàng)新藥迎來黃金時代����、中國科學家和工程師紅利,以及全球產(chǎn)業(yè)轉移等�����。其中�����,自2015年以來實施的一系列鼓勵創(chuàng)新藥政策����,影響了我國創(chuàng)新藥從研發(fā)到上市各個環(huán)節(jié)。(醫(yī)藥研發(fā)外包處行業(yè)景氣周期 數(shù)據(jù)來源:國泰君安證券研究)在MAH制度實施以前���,藥品上市申請和藥品生產(chǎn)申請����、藥品上市許可證和藥品生產(chǎn)許可證都必須由同一制藥廠商自己單獨完成藥品的上市銷售環(huán)節(jié),導致需要付出巨大的資金和時間成本���。但是�����,隨著MAH制度出臺后,生產(chǎn)證和注冊證分離����,藥品、器械再評價制度得到完善�����,不僅起到了鼓勵藥物創(chuàng)新的目的�����,也加速了商業(yè)化訂單承接�����、利好CMO企業(yè)發(fā)展,而且審評審批制度的改革���,也加速了創(chuàng)新藥的獲批進程����。對比來看���,醫(yī)療器械外包行業(yè)的痛點主要表現(xiàn)在臨床困難�����、銷售門檻高�����、專業(yè)人才匱乏���、知識產(chǎn)權/委托關系劃分等方面。首先���,醫(yī)療器械屬于多學科交叉�����、知識密集���、資金密集的高科技產(chǎn)業(yè)�����,必須配以精通多學科的復合型人才����,技術壁壘相當高���,而且不像新藥研發(fā)可以利用通用共享底層技術平臺,形成規(guī)?���;?/span>其次���,由于器械產(chǎn)品品類多且分類復雜����,訂單批量小,難以形成完整的產(chǎn)業(yè)鏈�����,而且更注重精密制造系統(tǒng)���、生產(chǎn)工藝�����,這也意味著CDMO企業(yè)需要維持更大的固定投入(資金����、實驗室設備����、生產(chǎn)設備等);再者���,醫(yī)療器械的銷售門檻更高���,銷售模式也更為特殊,不僅需要與醫(yī)院和醫(yī)生深度協(xié)調配合�����、臨床困難,而且法律法規(guī)多���、市場滲透期更長����,因此對醫(yī)療器械外包企業(yè)的服務項目廣度���、渠道資源���、營銷經(jīng)驗和交付能力的要求更高;最后�����,不同于知識產(chǎn)權劃分清晰的藥品研發(fā)�����,醫(yī)療器械產(chǎn)品保密系數(shù)高���,需要與醫(yī)療器械外包公司明確產(chǎn)權歸屬����、委托關系劃分等����,否則容易出現(xiàn)侵權問題。不過����,隨著醫(yī)療器械MAH制度的落地,也的確給醫(yī)療器械外包行業(yè)帶來了高速發(fā)展的契機���。2019年����,國家藥監(jiān)局將注冊人制度試點擴大到21個?����。ㄗ灾螀^(qū)或直轄市)�����,既“解綁”了醫(yī)療器械生產(chǎn)證和注冊證(意味著任何企業(yè)研發(fā)或者想擁有自己的產(chǎn)品���,可以委托研發(fā)���、委托生產(chǎn))���,也釋放出了CDMO/CMO的需求、打造一體化服務���,提高客戶黏性和市場競爭優(yōu)勢�����。例如����,CDMO企業(yè)從單純的產(chǎn)能輸出(CMO代工)轉變?yōu)椤岸ㄖ蒲邪l(fā)+定制生產(chǎn)”模式����,幫助更多醫(yī)療器械研發(fā)主體進行實際的技術轉化,縮短創(chuàng)新醫(yī)療器械研發(fā)上市周期���。據(jù)統(tǒng)計���,與自產(chǎn)相比,委托生產(chǎn)將節(jié)省12個月的時間����,節(jié)省超過80%的投入。此外�����,我國醫(yī)療器械外包市場滲透率還很低����,市場提升空間大。據(jù)統(tǒng)計����,美國CDMO的滲透率超過10%,而中國醫(yī)療器械CDMO的滲透率不足1%����。在MAH制度實施以前,國內醫(yī)療器械CRO的服務對象是歐美����、韓國等外企,主要代理外企醫(yī)療器械注冊���,協(xié)助其辦理注冊證���。另外����,也有出現(xiàn)像美敦力委托上海捷普科技代工生產(chǎn)的案例���,例如后者代工生產(chǎn)的手術動力系統(tǒng)���,就成為了上海醫(yī)療器械注冊人制度改革的第二個試點獲批產(chǎn)品,實現(xiàn)了進口產(chǎn)品本土轉化(進口產(chǎn)品國產(chǎn)化)的新模式�����。目前���,國內出現(xiàn)多種醫(yī)療器械CDMO業(yè)務類型�����,有專門為大企業(yè)做代工的����,也有在給企業(yè)代工的同時自己也研發(fā)產(chǎn)品的,海泰新光就屬于后者����。作為一家成立于2003年的老牌企業(yè)���,海泰新光最初以OEM模式起家供應LED器件����,之后成為美國醫(yī)療器械巨頭Stryker Corporation(史賽克)的供應商���,轉型為ODM模式�����,為史賽克提供光源模組����,于2021年在科創(chuàng)板掛牌上市����。回顧往年業(yè)績,海泰新光一直保持穩(wěn)健增長態(tài)勢:總營收從2017年的1.81億元增長至2021年的3.1億元,五年復合年增長率為11.36%�����;同期���,凈利潤從5109萬元增長至1.18億元����,CAGR為18.22%����。可見,凈利潤復合增速高于總營收復合增速����,主要系公司一直保持較強的盈利能力,其中����,銷售毛利率從2016年的54.78%一直穩(wěn)健增長至2021年的63.49%,與邁瑞醫(yī)療�����、開立醫(yī)療、萬東醫(yī)療���、天松醫(yī)療等從事醫(yī)用影像設備生產(chǎn)的企業(yè)相當����;銷售凈利率也從23.49%增長至37.83%���。雖然海泰新光業(yè)績保持穩(wěn)健,但如果拆分收入結構�����,會發(fā)現(xiàn)公司的主要收入來源于醫(yī)用內窺鏡器械業(yè)務(2021年實現(xiàn)營收2.28億元���,占公司收入比重高達73.53%)�����,毛利率達68.7%����,貢獻了公司79.57%的利潤比例����;其次���,光學產(chǎn)品2021年以8190萬元營收占公司收入比重26.45%,毛利率為48.98%���。深入來看���,海泰新光主要采用直銷的銷售模式,包括ODM模式����、OEM模式和自主品牌銷售三種類型,其中ODM產(chǎn)品(由公司自主設計����、開發(fā)和生產(chǎn),經(jīng)客戶確定滿足其應用標準后����,以客戶品牌銷售給用戶產(chǎn)品,俗稱“貼牌銷售”)�����,主要是高清內窺鏡器械,包括腹腔鏡�����、內窺鏡光源模組及內窺鏡攝像適配鏡頭以及小部分光學產(chǎn)品����,2021年實現(xiàn)業(yè)務收入2.14億元,占比69.2%���;OEM產(chǎn)品(由客戶提供產(chǎn)品圖紙�����、技術要求或樣品樣件,由公司進行生產(chǎn)并承擔產(chǎn)品相關的責任����,俗稱“代工生產(chǎn)”)主要集中在光學產(chǎn)品,2021年實現(xiàn)業(yè)務收入7584.54萬元���,占比24.50%���;自主品牌產(chǎn)品收入1959.29萬元���,占比6.33%,同比增加了66%���。值得注意的是����,海泰新光主要以海外收入為主(2021年實現(xiàn)營收2.47億元���,占比高達79.71%)���,其中核心客戶史賽克貢獻最大。最近四年����,史賽克占公司營業(yè)收入總額的比重均超過57%。海泰新光是史賽克首款熒光整機系統(tǒng)AIM的高清熒光腹腔鏡����、高清熒光攝像適配鏡頭和熒光光源模組的唯一供應商,兩家公司合作已有十余年���。從競爭格局看����,2019年史賽克占全球硬鏡的市場份額為27%,僅次于卡爾史托斯���,排名第二�����;同時����,史賽克占全球熒光內窺鏡市場份額高達78.4%����,排名第一����。與海外龍頭深度綁定,給海泰新光帶來了強勁的競爭優(yōu)勢����。另外,為了拓展國內市場����,海泰新光還通過持續(xù)的研發(fā)投入積極布局自主品牌�����,最近三年研發(fā)費用率分別為11.08%���、11.28%、11.24%�����、13.34%���。2021年�����,海泰新光在醫(yī)用內窺鏡產(chǎn)品上投入了較大的研發(fā)資源����,其中為美國客戶研發(fā)的4K熒光腹腔鏡已經(jīng)完成了研發(fā)和試生產(chǎn)過程����,準備在2022年下半年實現(xiàn)量產(chǎn)���;自主品牌的內窺鏡光源和1080P攝像系統(tǒng)已于2021年完成產(chǎn)品注冊并取得生產(chǎn)許可,4K熒光攝像系統(tǒng)也于2022年2月底獲得產(chǎn)品注冊和生產(chǎn)許可�����,目前已經(jīng)開始生產(chǎn)和銷售���。在國內硬鏡市場�����,由卡爾史托斯�����、奧林巴斯和史賽克等海外龍頭占據(jù)前三���,合計擁有超過70%市場份額,但也有包括邁瑞醫(yī)療�����、開立醫(yī)療�����、萬東醫(yī)療����、天松醫(yī)療等國內械企崛起,推動國產(chǎn)替代����。總結來看,憑借“技術+服務”的雙重優(yōu)勢以及與海外龍頭強強聯(lián)合�����,海泰新光無疑將奠定熒光內窺鏡領先優(yōu)勢���。除此以外�����,醫(yī)療器械外包行業(yè)還呈現(xiàn)出其他不同類型的業(yè)務模式�����。例如�����,臨床CRO龍頭泰格醫(yī)藥也有從事醫(yī)療器械CRO業(yè)務�����,全資子公司泰格捷通醫(yī)療器械服務業(yè)務范圍涵蓋醫(yī)療器械注冊����、臨床、體系����、檢測和咨詢等全服務,覆蓋了醫(yī)療器械的整個生命周期���。截至2020年底���,泰格醫(yī)藥搭建了60余個國內服務網(wǎng)點,覆蓋全國超過600家醫(yī)療器械臨床試驗服務機構�����,通過醫(yī)療器械注冊和臨床相關服務助力近200個產(chǎn)品取得注冊證書����,通過ISO9001年檢;2021年���,公司醫(yī)療器械臨床研究團隊進一步擴展數(shù)字健康和醫(yī)療機器人等新興服務領域����,通過醫(yī)療器械臨床研究團隊助力3個創(chuàng)新醫(yī)療器械和2個人工智能醫(yī)療軟件成功上市����。目前,泰格醫(yī)藥有341個正在進行的醫(yī)療器械項目�����,包括醫(yī)療器械和IVD臨床試驗�����、醫(yī)學監(jiān)查�����、方案設計和醫(yī)學撰寫。除此以外����,參考醫(yī)藥CXO企業(yè)成熟的商業(yè)模式,器械CRO也可以向上游CDMO領域延伸����,打造一體化服務,提高綜合競爭力優(yōu)勢����。例如,巨翊科技為國內領先的醫(yī)療器械CDMO技術服務及產(chǎn)品化解決方案平臺����,核心服務為產(chǎn)品研發(fā)服務及委托生產(chǎn)服務,服務范圍貫穿器械創(chuàng)新概念及技術研究�����、產(chǎn)品合作研發(fā)���,供應鏈管理���、到委托生產(chǎn)�����,產(chǎn)品臨床���、注冊及產(chǎn)品上市的全過程���。致眾科技專注于為醫(yī)療器械企業(yè)提供臨床試驗����、法規(guī)咨詢���、檢驗檢測���、委托研發(fā)、咨詢輔導及培訓等一體化解決方案���。領伯醫(yī)匯是為創(chuàng)新醫(yī)療器械產(chǎn)品提供CRO+CDMO+CMO全流程解決方案的第三方技術服務公司���,能夠提供從產(chǎn)品的檢測跟蹤、產(chǎn)品注冊����、產(chǎn)品臨床試驗���、產(chǎn)品的CDMO以及CMO全流程服務,涵蓋整個醫(yī)療器械全周期�����。結語:整體而言���,無論專注于CRO或CDMO單一業(yè)務���,還是打造一站式服務,這些醫(yī)療器械外包企業(yè)都有其優(yōu)勢之處����。不同的商業(yè)模式,會帶來不一樣的結果����。就目前而言,醫(yī)療器械外包行業(yè)仍處于起步階段����,可謂是百花齊放�����。至于未來誰能贏得“戰(zhàn)役”�����,交由時間來檢驗���。
文章來源:瞪羚社